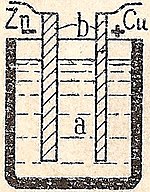
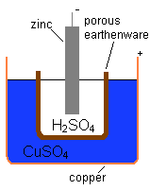
Электрохимическая ячейка, вызывающая протекание внешнего электрического тока, может быть создана с использованием любых двух различных металлов, поскольку металлы различаются по своей склонности терять электроны. Цинк охотнее теряет электроны, чем медь, поэтому помещение цинка и меди в растворы их солей может вызвать поток электронов через внешний провод, ведущий от цинка к меди. Поскольку атом цинка отдает электроны, он становится положительным ионом и переходит в водный раствор, уменьшая массу цинкового электрода. На стороне меди два полученных электрона позволяют ей превратить ион меди из раствора в незаряженный атом меди, который оседает на медном электроде, увеличивая его массу. Эти две реакции обычно записываются следующим образом
Zn(s) --> Zn2+(aq) + 2e
Cu2+(aq) + 2e- --> Cu(s)
Буквы в скобках напоминают, что цинк переходит из твердого состояния (s) в водный раствор (aq) и наоборот для меди. В языке электрохимии принято называть эти два процесса "полуреакциями", происходящими на двух электродах.
| Zn(s) -> Zn2+(aq) + 2e | | Полуреакция цинка классифицируется как окисление, поскольку он теряет электроны. Клемма, на которой происходит окисление, называется "анодом". Для батареи это отрицательный полюс. | |
| Полуреакция меди классифицируется как восстановление, так как она набирает электроны. Клемма, на которой происходит восстановление, называется "катодом". Для батареи это положительная клемма. | | Cu2+(aq) + 2e- -> Cu(s) |
Для того чтобы вольтов элемент продолжал вырабатывать внешний электрический ток, необходимо движение ионов сульфата в растворе справа налево, чтобы уравновесить поток электронов во внешней цепи. Сами ионы металла не должны перемещаться между электродами, поэтому какая-то пористая мембрана или другой механизм должны обеспечивать избирательное перемещение отрицательных ионов в электролите справа налево.
Для того чтобы заставить электроны перемещаться от цинкового электрода к медному, требуется энергия, а количество энергии на единицу заряда вольтова элемента называется электродвижущей силой (ЭДС) элемента. Энергия на единицу заряда выражается в вольтах (1 вольт = 1 джоуль/кулон).
Очевидно, что для получения энергии из ячейки необходимо получить больше энергии, выделяющейся при окислении цинка, чем требуется для восстановления меди. Ячейка может дать конечное количество энергии из этого процесса, процесс ограничен количеством материала, доступного либо в электролите, либо в металлических электродах. Например, если на стороне меди имеется один моль сульфат-ионов SO42-, то процесс ограничивается переносом двух молей электронов по внешней цепи. Величина электрического заряда, содержащегося в моле электронов, называется постоянной Фарадея и равна числу Авогадро, умноженному на заряд электрона:
Постоянная Фарадея = F = ANe = 6,022 x 1023 x 1,602 x 10-19 = 96,485 Кулон/моль
Выход энергии из вольтаического элемента определяется напряжением элемента, умноженным на количество молей перенесенных электронов, умноженное на постоянную Фарадея.
Выход электрической энергии = nFE
ЭДС ячейки Ecell может быть предсказана на основе стандартных электродных потенциалов для двух металлов. Для элемента цинк/медь при стандартных условиях расчетный потенциал элемента составляет 1,1 вольт.