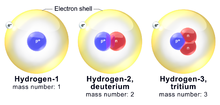
Атомы химического элемента могут существовать в различных типах. Они называются изотопами. Они имеют одинаковое количество протонов (и электронов), но разное количество нейтронов. Различные изотопы одного и того же элемента имеют разную массу. Масса - это слово, обозначающее, сколько вещества (или материи) у чего-то есть. Вещи с разной массой имеют разную массу. Поскольку у разных изотопов разное количество нейтронов, они не все весят одинаково или имеют разную массу.
Различные изотопы одного и того же элемента имеют один и тот же атомный номер. Они имеют одинаковое количество протонов. Атомный номер определяется количеством протонов. Изотопы имеют разные массовые числа, потому что они имеют разное количество нейтронов.
Слово изотоп, означающее в одном и том же месте, происходит от того, что изотопы находятся в одном и том же месте на периодической таблице.
В нейтральном атоме число электронов равно числу протонов. Изотопы одного и того же элемента также имеют одинаковое число электронов и электронную структуру. Потому что то, как атом действует, определяется его электронной структурой, изотопы почти те же самые химически, но физически отличаются от своих первоначальных атомов.
Более тяжелые изотопы реагируют химически медленнее, чем более легкие изотопы того же элемента. Этот "массовый эффект" больше для протия (1H) и дейтерия (2H), поскольку дейтерий имеет в два раза большую массу протия. Для более тяжелых элементов относительное соотношение атомной массы между изотопами значительно меньше, а массовый эффект обычно мал.