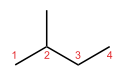Структурный изомер
Структурная изомерия (IUPAC называет ее конституционной изомерией) - это разновидность изомерии. Два химических вещества в этой изомерии имеют одинаковую молекулярную формулу, но молекулы связаны друг с другом в разном порядке. Противоположностью структурной изомерии является стереоизомерия. Существует много слов, обозначающих структурные изомеры.
Существует три вида конституционных изомеров. Это скелетные изомеры, позиционные изомеры и функциональные изомеры. Позиционные изомеры также называются региоизомерами. Таутомеры также являются разновидностью функциональных изомеров.
Скелетная изомерия
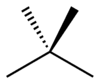
При скелетной изомерии, или изомерии цепи, компоненты скелета (обычно углерод) перестраиваются, образуя различные структуры. У пентана есть три изомера. Это н-пентан (часто называемый просто "пентан"), изопентан (метилбутан) и неопентан (диметилпропан).
| Скелетная изомерия пентана | ||
|
|
|
|
| н-Пентан | Изопентан | Неопентан |
Позиционная изомерия
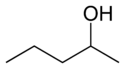
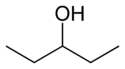
При позиционной изомерии функциональная группа или другой заместитель меняет свое положение в родительской структуре. В приведенной ниже таблице гидроксильная группа может находиться в трех различных положениях на цепи н-пентана, образуя три различных соединения.
| Пример позиционной изомерии | ||
|
|
|
|
| 1-пентанол | 2-пентанол | 3-пентанол |
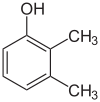
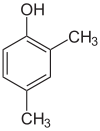
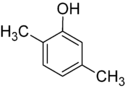
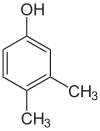
Существует множество ароматических изомеров, поскольку заместители могут быть расположены на разных частях бензольного кольца. Существует только один изомер фенола или гидроксибензола, но крезол или метилфенол имеет три изомера, в которых дополнительная метильная группа может быть расположена в трех разных местах кольца. Ксиленол имеет одну гидроксильную группу и две метильные группы, и всего существует 6 изомеров.
| Позиционные изомеры ксиленола | ||
|
|
|
|
| 2,3-ксиленол | 2,4-Ксиленол | 2,5-Ксиленол |
|
|
|
|
| 2,6-ксиленол | 3,4-Ксиленол | 3,5-ксиленол |
Изомерия функциональных групп
Функциональные изомеры являются одним из структурных изомеров. Два соединения в функциональной изомерии имеют одинаковую молекулярную формулу (номер каждого атома одинаков, например, циклогексан:C
6H
12 и 1-гексен: C
6H
12). Но атомы соединены другими способами, так что группировки отличаются. Мы называем эти группы атомов функциональными группами, функциями или обществами. По-другому можно сказать, что два соединения с одинаковой молекулярной формулой, но с разными функциональными группами, являются функциональными изомерами.
Например, химическая формула циклогексана и 1-гексена - C6 H12 . Мы называем их изомерами по функциональной группе, потому что циклогексан - это циклоалкан, а гекс-1-ен - алкен.
| Пример изомерии функциональных групп | |
|
|
|
| 1-гексен | |
Для того чтобы две молекулы были функциональными изомерами, они должны содержать ключевые группы атомов, расположенные определенным образом. Некоторые из лучших примеров взяты из органической химии. C2 H6 O - это молекулярная формула. В зависимости от того, как расположены атомы, она может представлять два различных соединения диметиловый эфир CH3 -O-CH3 или этанол CH3 CH2 -O-H. Диметиловый эфир и этанол являются функциональными изомерами. Первый является эфиром. Функциональная цепочка углерод-кислород-углерод называется эфиром. Второй - спирт. Функциональность углеродной цепи-кислород-водород называется спиртом.
Если функциональные свойства остаются неизменными, но их расположение меняется, структурные изомеры не являются функциональными изомерами. 1-пропанол и 2-пропанол - структурные изомеры, но они не являются функциональными изомерами. Оба они являются спиртами. Функциональная группа (углеродная цепь-O-H) присутствует в обоих этих соединениях, но они не одинаковы.
Хотя некоторые химики используют термины структурный изомер и функциональный изомер как взаимозаменяемые, не все структурные изомеры являются функциональными изомерами.
Функциональные изомеры чаще всего идентифицируются в химии с помощью инфракрасной спектроскопии. Инфракрасное излучение соответствует энергиям, связанным в первую очередь с молекулярной вибрацией. Функциональные свойства спирта имеют очень отчетливую вибрацию, называемую OH-растяжением, которая обусловлена водородной связью. Все спирты в жидком и твердом состоянии поглощают инфракрасное излучение при определенных длинах волн.
Соединения с одинаковыми функциональными группами поглощают определенные длины волн инфракрасного света из-за колебаний, связанных с этими группами. Фактически, инфракрасный спектр делится на две области. Первая часть называется областью функциональных групп. Диметиловый эфир и этанол имеют разные инфракрасные спектры в области функциональных групп.
Вторая часть инфракрасного спектра называется областью отпечатков; она связана с типами движения, допускаемыми симметрией молекулы и зависящими от энергий связей. Область отпечатков пальцев более специфична для отдельного соединения. Хотя 1-пропанол и 2-пропанол имеют схожие инфракрасные спектры в области функциональных групп, они отличаются в области отпечатков пальцев.
Проще говоря, функциональные изомеры - это структурные изомеры, имеющие различные функциональные группы, например, спирт и эфир.
Подсчет изомеров
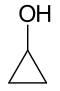
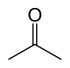
В качестве примера подсчета изомеров можно привести 7 структурных изомеров с молекулярной формулой C3 H6 O, каждый из которых имеет различные связи и стабилен на воздухе при температуре окружающей среды. Еще два структурных изомера являются энольными таутомерами карбонильных изомеров, но они не стабильны.
| Молекулярная структура | Температура плавления (°C) | Температура кипения (°C) | Комментарий | |
| Аллиловый спирт |
| -129 | 97 | |
| Циклопропанол |
| 101-102 | ||
| Пропаналь |
| - 81 | 48 | Таутомерия с (E)-1-пропенолом и (Z)-1-пропенолом |
| Ацетон |
| - 94.9 | 56.53 | Таутомерия с 2-пропенолом |
| Оксетан |
| - 97 | 48 | |
| Оксид пропилена |
| - 112 | 34 | Может быть разделен на два энантиомера |
| Метилвиниловый эфир |
| - 122 | 6 |
искать