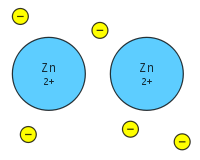
Металлическая связь - это обмен многими отделенными электронами между многими положительными ионами, где электроны действуют как "клей", придавая веществу определенную структуру. Это отличается от ковалентной или ионной связи. Металлы имеют низкую энергию ионизации. Поэтому валентные электроны могут делокализоваться по всему металлу. Делокализованные электроны не связаны с определенным ядром металла, вместо этого они свободно перемещаются по всей кристаллической структуре, образуя "море" электронов.
Между электронами и положительными ионами в металле существует сильная притягательная сила. Поэтому металлы часто имеют высокую температуру плавления или кипения. Принцип аналогичен принципу ионных связей.
Металлические связи вызывают многие свойства металлов, такие как прочность, пластичность, пластичность, блеск, тепло- и электропроводность.
Поскольку электроны движутся свободно, металл обладает некоторой электропроводностью. Это позволяет энергии быстро проходить через электроны, генерируя электрический ток. Металлы проводят тепло по той же причине: свободные электроны могут передавать энергию быстрее, чем другие вещества с электронами, зафиксированными в положении. Немногие неметаллы также проводят электричество: графит (потому что, как и металлы, он имеет свободные электроны), и ионные соединения, которые расплавляются или растворяются в воде, которые имеют свободные движущиеся ионы.
Металлические связи имеют по крайней мере один валентный электрон, который они не делят с соседними атомами, и они не теряют электроны для образования ионов. Вместо этого внешние энергетические уровни (атомные орбиты) атомов металла перекрываются. Они схожи с ковалентными связями. Не все металлы имеют металлическую связь. Например, ионы ртути (Hg2+
2) формируют ковалентные связи металл-металл.
Сплав - это раствор металлов. Большинство сплавов блестит так же, как и чистые металлы.