Модель сливового пудинга
Модель сливового пудинга - это ранняя (и неправильная) модель атома 20-го века. Она была предложена Дж. Дж. Томсоном в 1904 году, после открытия электрона, но до открытия атомного ядра. В то время ученые знали, что в атоме есть положительный заряд, который уравновешивает отрицательные заряды электронов, делая атом нейтральным, но они не знали, откуда берется положительный заряд. Модель Томсона показывала атом, имеющий положительно заряженную среду, или пространство, с отрицательно заряженными электронами внутри среды. Вскоре после его предложения модель назвали моделью "сливового пудинга", потому что положительная среда была похожа на пудинг, внутри которого находились электроны, или сливы.

Пример модели Томсона
Развитие в современную атомную модель
Модель Резерфорда
В принципе, в 1909 году, вскоре после того, как была предложена модель Томсона, Ганс Гейгер и Эрнест Марсден провели эксперимент с тонкими листами золота, чтобы проверить модель Томсона. Их профессор, Эрнест Резерфорд, ожидал, что результаты докажут правоту Томсона, но результаты оказались совсем не такими, как они ожидали. В 1911 году Резерфорд обнаружил, что положительные заряды исходят от крошечных частиц, называемых протонами, что протоны находятся в крошечном центре, называемом ядром, а электроны вращаются вокруг ядра.
модель Бора
Модель Резерфорда была довольно простой, но неправильной, потому что электроны имеют заряд, и они должны притягиваться к положительно заряженному ядру. В 1913 году Нильс Бор добавил в атомную модель "энергетические уровни". Электроны не падают в ядро, потому что они находятся на энергетических уровнях, и для перехода на более высокие энергетические уровни требуется дополнительная энергия, а для перехода на более низкие энергетические уровни необходимо высвобождение энергии. Невозможно изменить энергетическое состояние без изменения энергии электрона. Если в электрон попадет фотон (частица, переносящая электромагнитное излучение), он получит дополнительную энергию и перейдет на более высокий энергетический уровень (изменит состояние), а затем перейдет обратно на более низкий энергетический уровень, высвободив содержащуюся в нем энергию. Эта новая модель была названа моделью Бора или моделью Резерфорда-Бора. Это добавило совершенно новую отрасль науки: Квантовая физика.
Квантовая модель
В 1926 году Эрвин Шредингер использовал идею о том, что электроны действуют как волны, так и частицы, это известно как дуализм волна-частица. Это добавило совершенно новый слой к атомной модели и квантовой физике. У частицы можно узнать, где она находится в пространстве, если наблюдать (смотреть) на нее. Но в случае волны она находится повсюду, поэтому вы не можете определить, где именно она находится. Это известно как квантовая неопределенность. В случае электрона вы можете знать только вероятность того, что он находится в том или ином месте, поскольку он является как волной, так и частицей. (См. диаграмму выше)
Изображение, показывающее, как электрон меняет энергетический уровень, получает и высвобождает энергию в виде фотонов.
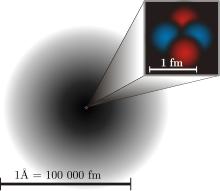
Здесь показана текущая атомная модель. Черная штриховка вокруг атома показывает вероятность нахождения там электрона. Чем она темнее, тем больше шансов найти электрон в этом месте.
Похожие страницы
- Атомная теория
- Квантовая механика
- J. Дж. Томсон
- Эрнест Резерфорд
- Нильс Бор
- Эрвин Шредингер
искать