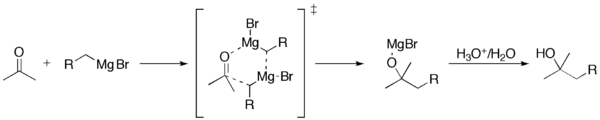
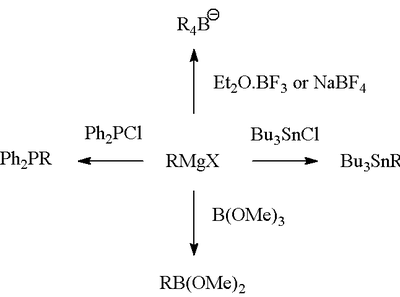
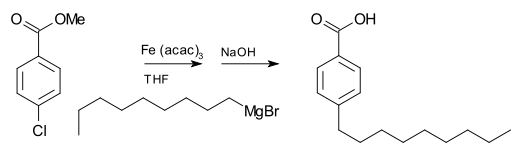
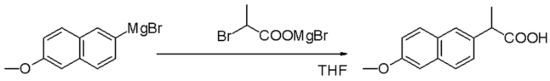
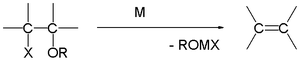
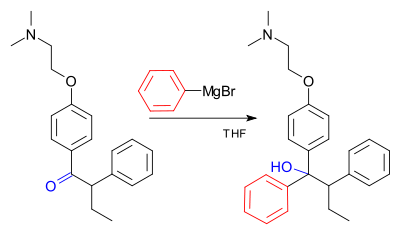
Реакция Гриньяра (произносится /ɡriɲar/) - это металлоорганическая химическая реакция, в которой алкил- или арил-магниевые галогениды (реагенты Гриньяра) атакуют электрофильные атомы углерода, присутствующие в полярных связях (например, в карбонильной группе, как в примере, показанном ниже). Реагенты Гриньяра действуют как нуклеофилы. В результате реакции Гриньяра образуется связь углерод-углерод. Она изменяет гибридизацию о центре реакции. Реакция Гриньяра является важным инструментом в образовании углерод-углеродной связи. Она также может образовывать связи углерод-фосфор, углерод-олово, углерод-кремний, углерод-бор и другие связи углерод-гетероатом.
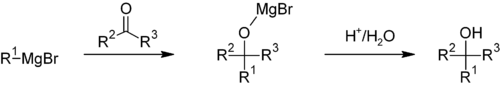
Это нуклеофильная реакция добавления металлоорганических веществ. Высокое значение pKa алкильного компонента (pKa = ~ 45) делает реакцию необратимой. Реакции Гриньяра не являются ионными. Реагент Гриньяра существует в виде металлоорганического кластера (в эфире).
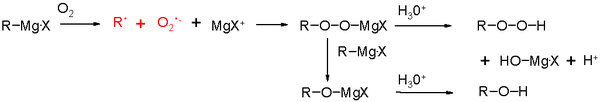
Недостатком реагентов Гриньяра является то, что они легко реагируют с протическими растворителями (такими как вода), или с функциональными группами с кислыми протонами, такими как спирты и амины. Влажность воздуха может изменять выход реагента Гриньяра из магния и алкилгалогенида. Одним из многих методов, используемых для исключения воды из атмосферы реакции, является пламя-высушивание реакционного сосуда для испарения всей влаги, которая затем запечатывается, чтобы предотвратить возврат влаги. Затем химики используют ультразвук для активации поверхности магния, чтобы он потреблял любую присутствующую воду. Это может позволить реагентам Гриньяра формироваться с меньшей чувствительностью к присутствию воды.
Другим недостатком реагентов Гриньяра является то, что они не могут легко образовывать углерод-углеродные связи, реагируя с алкилгалогенидами по механизмуSN2.
Франсуа Огюст Виктор Гриньяр обнаружил реакции и реагенты Гриньяра. Они названы в честь этого французского химика (Университет Нанси, Франция), который за эту работу был удостоен Нобелевской премии по химии 1912 года.