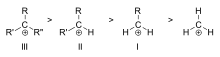
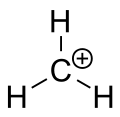
Карбокатион - это ион с положительно заряженным атомом углерода. Заряженный атом углерода в карбокатионе является "секстетом" (то есть, он имеет только шесть электронов в своей внешней валентной оболочке вместо восьми валентных электронов). Атомы углерода с восемью валентными выборами обладают максимальной стабильностью (правило октета). Поэтому карбокатионы часто являются реакционноспособными, стремясь заполнить октет валентных электронов, а также вернуть себе нейтральный заряд. Логика подсказывает, что карбокатион имеет sp3 гибридизацию с пустой sp 3орбиталью, дающей положительный заряд. Однако реакционная способность карбокатиона больше похожа на sp-гибридизацию2 с тригональной планарной геометрией молекулы.
Карбкатион




Определения
Раньше карбокатион часто называли карбониевым ионом, но химики сомневаются в точном значении этого слова. В современной химии карбокатион - это любой положительно заряженный атом углерода. Было предложено два особых типа: карбениевые ионы - трехвалентные, а карбониевые - пятивалентные или шестивалентные. В учебниках университетского уровня карбокатионы обсуждаются только как карбениевые ионы, или же карбокатионы обсуждаются с мимолетной ссылкой на более старое выражение карбениевый ион или карбениевые и карбониевые ионы. Один учебник до сих пор придерживается старого названия карбониевого иона для карбениевого иона и сохраняет фразу гипервалентный карбениевый ион для CH5+.
История
В 1891 году Г. Мерлинг сообщил, что он добавил бром к тропилидену (циклогептатриену) и затем нагрел продукт, получив кристаллическое, растворимое в воде вещество, C
7H
7Br. Он не предложил его структуру, однако Доринг и Нокс убедительно показали, что это был бромид тропилия (циклогептатриенилия). Согласно правилу Хюккеля, этот ион должен быть ароматическим.
В 1902 году Норрис и Керман независимо друг от друга обнаружили, что бесцветный трифенилметанол дает темно-желтые растворы в концентрированной серной кислоте. Хлорид трифенилметил аналогичным образом образует оранжевые комплексы с хлоридами алюминия и олова. В 1902 году Адольф фон Байер отметил солеподобный характер образующихся соединений.
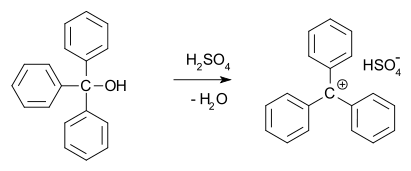
Он назвал связь между цветом и образованием соли галохромией, ярким примером которой является малахитовый зеленый.
Карбокатионы являются реактивными промежуточными соединениями во многих органических реакциях. Эта идея, впервые предложенная Юлиусом Штиглицем в 1899 году, была развита Гансом Меервейном в 1922 году в его исследовании перегруппировки Вагнера-Меервейна. Было также установлено, что карбокатионы участвуют в реакции S1N, реакции E1 и в реакциях перегруппировки, таких как сдвиг Уитмора 1,2. Химический истеблишмент неохотно принимал понятие карбокатиона, и долгое время журнал Американского химического общества отказывался от статей, в которых они упоминались.
Первый спектр ЯМР стабильного карбокатиона в растворе был опубликован Доерингом и др. в 1958 году. Это был ион гептаметилбензония, полученный путем обработки гексаметилбензола хлористым метилом и хлористым алюминием. Стабильный 7-норборнадиенильный катион был получен Стори и др. в 1960 году путем реакции норборнадиенилхлорида с тетрафторборатом серебра в диоксиде серы при -80 °C. Спектр ЯМР показал, что он был неклассически мостиковым (первый наблюдаемый стабильный неклассический ион).
В 1962 году Олах непосредственно наблюдал терт-бутилкарбокатион с помощью ядерного магнитного резонанса как стабильный вид при растворении терт-бутилфторида в магической кислоте. О ЯМР катиона норборнила впервые сообщили Шлейер и др., а Сондерс и др. показали, что он подвергается протонному скремблированию через барьер.
Свойства
В органической химии карбокатион часто является объектом нуклеофильной атаки со стороны нуклеофилов, таких как гидроксил (OH−) ионы или ионы галогенов.
Карбокатионы классифицируются как первичные, вторичные или третичные в зависимости от количества атомов углерода, связанных с ионизированным углеродом. Первичные карбокатионы имеют один или ноль углеродов, присоединенных к ионизированному углероду, вторичные карбокатионы имеют два углерода, присоединенных к ионизированному углероду, а третичные карбокатионы имеют три углерода, присоединенных к ионизированному углероду.
Стабильность карбокатиона увеличивается с числом алкильных групп, связанных с несущим заряд углеродом. Третичные карбокатионы более стабильны (и образуются легче), чем вторичные карбокатионы; первичные карбокатионы крайне нестабильны, поскольку, в то время как ионизированные углероды высшего порядка стабилизированы гиперконъюгацией, незамещенные (первичные) углероды не стабилизированы. Поэтому такие реакции, как реакция S1N и реакция элиминирования E1, обычно не происходят, если образуется первичный карбокатион. Исключение составляют случаи, когда рядом с ионизированным углеродом находится углерод-углеродная двойная связь. Такие катионы, как аллил-катион CH=CH-CH22+ и бензил-катион 6CH-CH52+, более стабильны, чем большинство других карбокатионов. Молекулы, которые могут образовывать аллильные или бензильные карбокатионы, особенно реакционноспособны.
Карбокатионы подвергаются реакциям перегруппировки из менее стабильных структур в такие же или более стабильные с константами скорости более 10/сек9. Этот факт усложняет синтетические пути получения многих соединений. Например, при нагревании 3-пентанола с водной HCl первоначально образовавшийся 3-пентильный карбокатион перестраивается в статистическую смесь 3-пентила и 2-пентила. Эти катионы реагируют с хлорид-ионом с образованием примерно 1/3 3-хлорпентана и 2/3 2-хлорпентана.
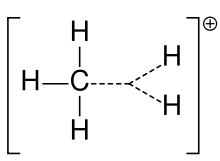
Некоторые карбокатионы, такие как катион норборнила, демонстрируют более или менее симметричную трехцентровую связь. Катионы такого рода называют неклассическими ионами. Разница в энергии между "классическими" карбокатионами и "неклассическими" изомерами часто очень мала, и обычно энергия активации при переходе между "классическими" и "неклассическими" структурами незначительна, если вообще существует. Неклассическая" форма 2-бутилкарбокатиона - это, по сути, 2-бутен с протоном непосредственно над центром двойной связи углерод-углерод. "Неклассические" карбокатионы когда-то были предметом больших споров. Одним из величайших вкладов Джорджа Олаха в химию было разрешение этих разногласий.
Специфические карбокатионы
Циклопропилкарбинильные катионы могут быть изучены методом ЯМР:
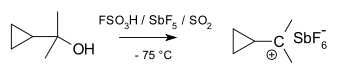
В спектре ЯМР диметильного производного обнаружены два неэквивалентных сигнала для двух метильных групп, указывающих на то, что молекулярная конформация этого катиона не перпендикулярна (как в A), а биссектрисальна (как в B) с пустой p-орбиталью и циклопропильной кольцевой системой в одной плоскости:
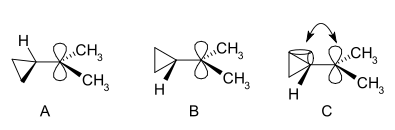
С точки зрения теории изогнутых связей, это предпочтение объясняется предположением о благоприятном перекрывании орбиталей между заполненными изогнутыми связями циклопропана и пустой p-орбиталью.
Вопросы и ответы
В: Что такое карбокатион?
О: Карбокатион - это ион с положительно заряженным атомом углерода.
В: Какова внешняя валентная оболочка карбокатиона?
О: Внешняя валентная оболочка карбокатиона имеет только шесть электронов вместо стабильных восьми валентных электронов.
В: Почему карбокатионы часто бывают реакционноспособными?
О: Карбокатионы часто реакционноспособны, поскольку они стремятся заполнить октет валентных электронов, а также вернуть себе нейтральный заряд.
В: Какова максимальная стабильность для атомов углерода?
О: Максимальная стабильность атомов углерода достигается, когда они имеют восемь валентных электронов.
В: Что такое секстет в химии?
О: Секстет - это термин, используемый для описания атома углерода в карбокатионе, который имеет только шесть электронов в своей внешней валентной оболочке вместо стабильных восьми валентных электронов.
В: Что такое гибридизация и молекулярная геометрия карбокатиона?
О: Хотя логика подсказывает, что карбокатионы имеют sp3 гибридизацию с пустой sp3 орбиталью, дающей положительный заряд, их реакционная способность больше напоминает sp2 гибридизацию с тригональной планарной молекулярной геометрией.
В: Что такое правило октета?
О: Правило октета - это принцип в химии, который гласит, что атомы стремятся образовывать химические связи с другими атомами, которые позволяют обоим атомам иметь стабильный набор из восьми валентных электронов.