Реакция S1N - это реакция замещения в органической химии. "SN" означает нуклеофильное замещение, а "1" означает тот факт, что на этапе, определяющем скорость, участвует только одна молекула (унимолекулярная). В реакции участвует промежуточный карбокатион. Некоторые распространенные реакции S1N - это реакции вторичных или третичных алкилгалогенидов в сильно основных условиях или, в сильно кислых условиях, со вторичными или третичными спиртами. С первичными алкилгалогенидами происходит альтернативная реакция S2N. Среди химиков-неоргаников реакция S1N часто известна как диссоциативный механизм. Кристофер Ингольд и др. впервые предложили механизм реакции в 1940 году.
SN1-реакция
Механизм
Примером реакции, протекающей по механизму реакции S1N, является гидролиз терт-бутилбромида водой с образованием терт-бутилового спирта:
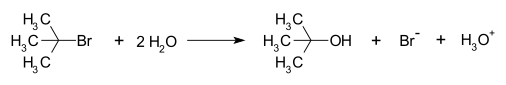
Эта реакция S1N происходит в три этапа:
- Образование трет-бутилкарбокатиона путем отрыва уходящей группы (бромид-аниона) от атома углерода; эта стадия медленная и обратимая.
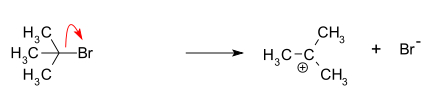
- Нуклеофильная атака: карбокатион вступает в реакцию с нуклеофилом. Если нуклеофил - нейтральная молекула (то есть растворитель), для завершения реакции требуется третий этап. Когда растворителем является вода, промежуточным продуктом является ион оксония. Эта стадия реакции протекает быстро.

- Депротонирование: Удаление протона на протонированном нуклеофиле водой, действующей как основание, с образованием спирта и иона гидрония. Этот этап реакции протекает быстро.
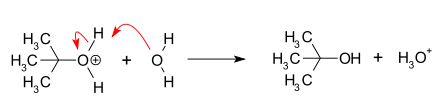
Поскольку первый шаг является узким местом или "шагом, определяющим скорость", химики классифицируют весь механизм реакции как S1N. Для этого шага требуется только одна молекула.
Сфера применения реакции
Иногда молекула может реагировать по механизму S1N или S2N. Механизм S1N побеждает в этом соревновании, когда центральный атом углерода окружен громоздкими группами, поскольку такие группы стерически препятствуют реакции S2N. Кроме того, громоздкие заместители на центральном углероде увеличивают скорость образования карбокатиона, так как происходит ослабление стерического напряжения. Образующийся карбокатион также стабилизируется за счет индуктивной стабилизации и гиперконъюгации от присоединенных алкильных групп. Согласно постулату Хаммонда-Леффлера, это также увеличивает скорость образования карбокатиона. Таким образом, механизм S1N доминирует в реакциях на третичных алкильных центрах и далее наблюдается на вторичных алкильных центрах в присутствии слабых нуклеофилов.
Примером реакции, протекающей по схеме S1N, является синтез 2,5-дихлор-2,5-диметилгексана из соответствующего диола с помощью концентрированной соляной кислоты:
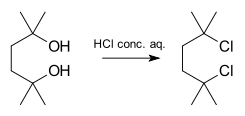
По мере увеличения альфа- и бета-заместителей по отношению к уходящим группам реакция переходит от S2N к S1N.
Стереохимия
Промежуточный карбокатион, образующийся на лимитирующей по скорости стадии реакции, представляет собой sp-гибридизованный2 углерод с тригональной планарной геометрией молекулы. Это позволяет использовать два различных пути для нуклеофильной атаки, по одному с каждой стороны планарной молекулы. Если ни один из путей не является предпочтительным, эти два пути будут использоваться одинаково, давая рацемическую смесь энантиомеров, если реакция происходит на стереоцентре. Это показано ниже на примере реакции S1N S-3-хлор-3-метилгексана с йодид-ионом, в результате которой образуется рацемическая смесь 3-йод-3-метилгексана:
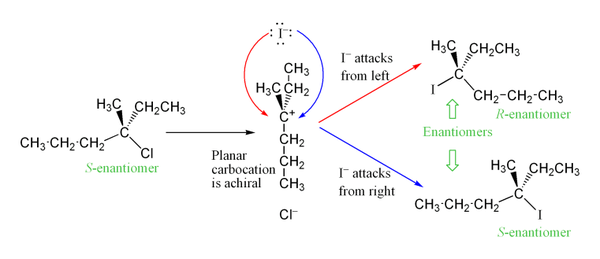
Однако может наблюдаться избыток одного стереоизомера, поскольку уходящая группа может оставаться вблизи промежуточного карбокатиона в течение короткого времени и блокировать нуклеофильную атаку. Это очень отличается от механизма S2N, который не смешивает стереохимию продукта (стереоспецифический механизм). Механизм S2N всегда инвертирует стереохимию молекулы.
Побочные реакции
Двумя распространенными побочными реакциями являются реакции элиминирования и карбокатионной перегруппировки. Если реакция протекает в теплых или горячих условиях (которые способствуют увеличению энтропии), то, скорее всего, будет преобладать элиминирование E1, что приведет к образованию алкена. При более низких температурах реакции S1N и E1 являются конкурентными. Таким образом, становится трудно отдать предпочтение одной из них перед другой. Даже если реакция проводится на холоде, может образоваться некоторое количество алкена. Если попытаться провести реакцию S1N с использованием сильно основного нуклеофила, такого как гидроксид или метоксид-ион, алкен снова образуется, на этот раз путем элиминирования E2. Это особенно верно, если реакция протекает при нагревании. И наконец, если промежуточный карбокатион может перестроиться в более стабильный карбокатион, он даст продукт, полученный из более стабильного карбокатиона, а не простой продукт замещения.
Влияние растворителей
Растворители изменяют скорость реакции. Поскольку реакция S1N включает образование нестабильного промежуточного карбокатиона на этапе, определяющем скорость, все, что может помочь этому, ускорит реакцию. Обычными растворителями являются как полярные (для стабилизации ионных промежуточных продуктов в целом), так и протические (для сольватации уходящей группы в частности). Типичные полярные протические растворители включают воду и спирты, которые также выступают в качестве нуклеофилов.
Шкала Y соотносит скорость реакции сольволиза любого растворителя (k) со скоростью реакции стандартного растворителя (80% v/v этанол/вода) (k0) через
log ( k k ) 0= m Y {\displaystyle \log {\left({\frac {k}{k_{0}}}}\right)}=mY\,}
с m - константой реактива (m = 1 для хлористого терт-бутила),
- Y параметр растворителя, и
- k0 - скорость реакции при использовании растворителя 80% этанола (измеряется по объему).
Например, 100% этанол дает Y = -2,3, 50% этанол в воде Y = +1,65 и 15% концентрация Y = +3,2.
Вопросы и ответы
В: Что означает "SN" в реакции SN1?
О: "SN" означает нуклеофильное замещение.
В: Что означает "1" в реакции SN1?
О: "1" означает тот факт, что в определяющей скорость реакции участвует только одна молекула (унимолекулярная).
В: К какому типу реакций относится SN1?
О: SN1 - это реакция замещения.
В: Какой промежуточный продукт участвует в реакции SN1?
О: В реакции SN1 участвует промежуточный карбокатион.
В: При каких условиях происходят обычные реакции SN1?
О: Обычные реакции SN1 происходят со вторичными или третичными алкилгалогенидами в сильноосновных условиях, или со вторичными или третичными спиртами в сильнокислых условиях.
В: Какая альтернативная реакция происходит с первичными алкилгалогенидами?
О: С первичными алкилгалогенидами происходит альтернативная реакция SN2.
В: Кто и в каком году впервые предложил механизм реакции SN1?
О: Кристофер Ингольд и др. впервые предложили механизм реакции SN1 в 1940 году.
