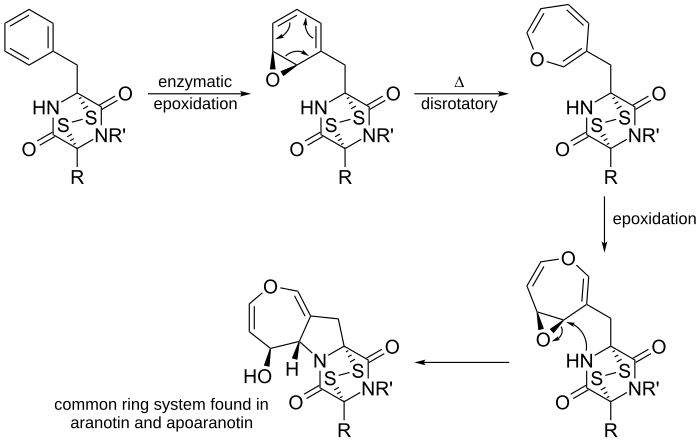
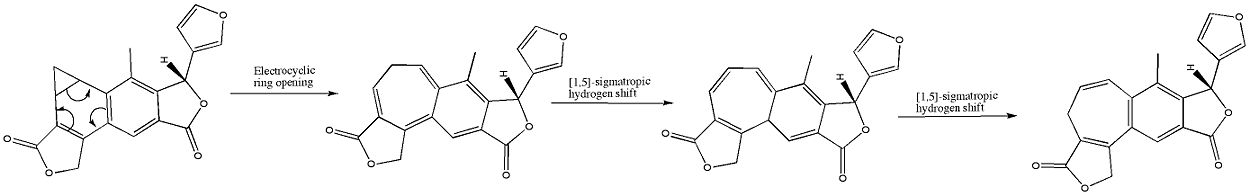
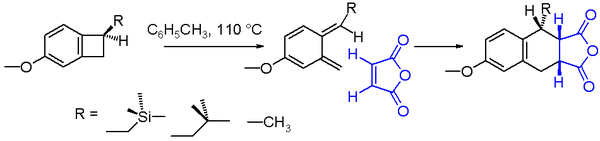
В органической химии электроциклическая реакция является одним из видов перициклической реакции перегруппировки. Реакция является электроциклической, если в результате одна пи-связь становится одной сигма-связью или одна сигма-связь становится пи-связью. Электроциклические реакции обладают следующими свойствами:
- электроциклические реакции управляются светом (фотоиндуцированные) или теплом (тепловые)
- режим реакции определяется количеством пи-электронов в части с более пи-связью
- электроциклическая реакция может закрыть кольцо (электроциклизация) или открыть кольцо.
- Стереоспецифичность определяется формированием вращательного или дезротирующего переходного состояния, предсказываемого правилами Вудфорд-Хоффмана.
Торквоселективность в электроциклической реакции относится к тому направлению, в котором вращаются заменители. Например, заменители в реакции с вращением все еще могут вращаться в двух направлениях. При этом образуется смесь двух продуктов, которые являются зеркальным отражением друг друга (энантиомерные продукты). Реакция, которая является торквоселективной, ограничивает одно из этих направлений вращения (частично или полностью) для получения продукта в энантиомерном избытке (когда один стереоизомер производится намного больше, чем другой).
Химиков интересуют электроциклические реакции, поскольку геометрия молекул подтверждает ряд предсказаний, сделанных химиками-теоретиками. Они подтверждают сохранение молекулярной орбитальной симметрии.
Реакция циклизации Назарова - это электроциклическая реакция, которая замыкает кольцо. Она преобразует дивинилкетоны в циклопентеноны. (Она была открыта Иваном Николаевичем Назаровым (1906-1957).)
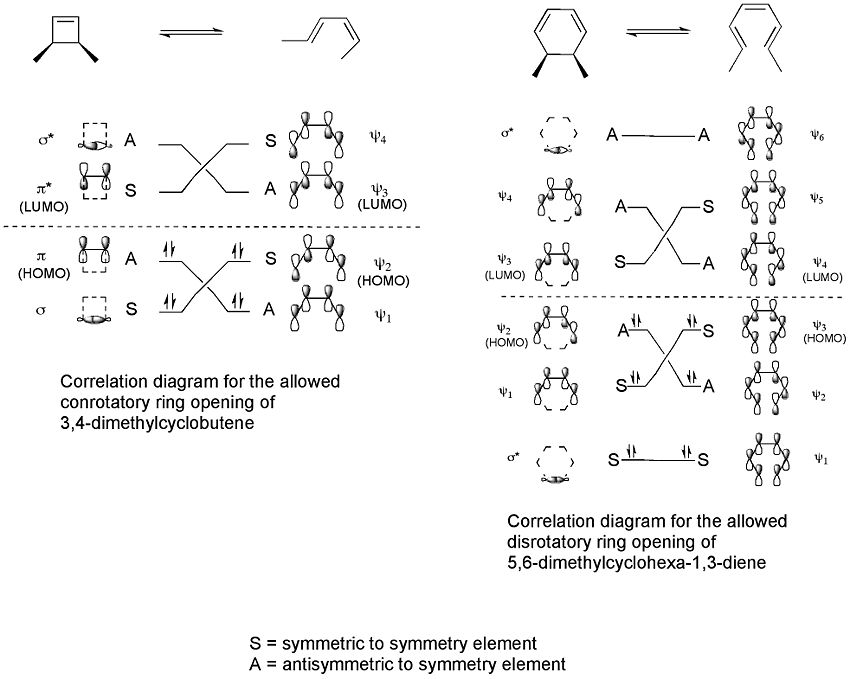
Примером может служить термическая реакция открытия кольца из 3,4-диметилциклобутена. Изомер цис дает только цис, транс-2,4-гексадиен. Но транс-изомер дает транс,транс-диен:
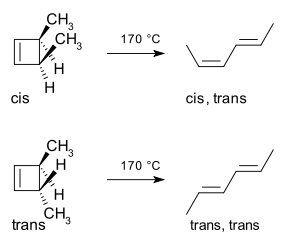
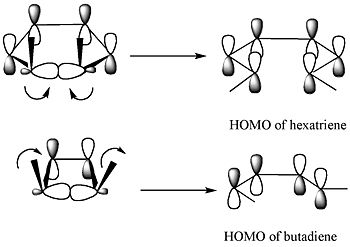
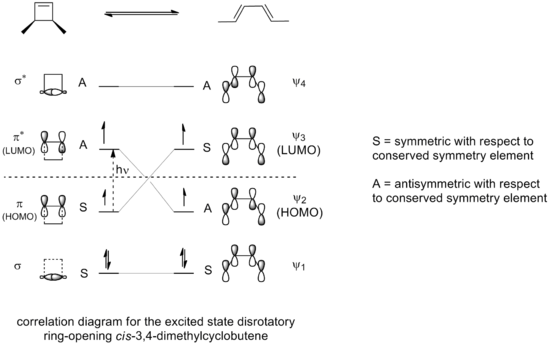
Погранично-орбитальный метод объясняет, как работает эта реакция. Сигма-связь в реагенте будет открыта таким образом, что результирующие р-орбиталы будут иметь ту же симметрию, что и самый высокий оккупированный молекулярный орбитал (HOMO) продукта (бутадиен). Это может произойти только при открытии вращательного кольца, что приведет к появлению противоположных признаков для двух долей на разорванных концах кольца. (При дезориентационном открытии кольца образуется антисвязка.) Это показано на следующей диаграмме:
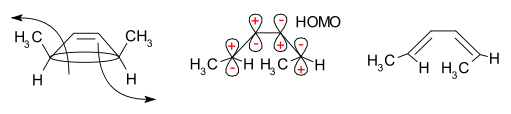
Стереоспецифичность результата зависит от того, проходит ли реакция через вращательный или дезориентационный процесс.