Сигматропная реакция в органической химии - перициклическая реакция. Сигматропическая реакция не использует катализатор и включает в себя одну молекулу (некатализируемый внутримолекулярный процесс). Она превращает одну σ-связку в другую σ-связку. Название сигматропа является результатом соединения давно принятого названия "сигма" для одноуглерод-углеродных связей и греческого слова tropos, означающего "поворот". Это реакция перестройки, которая означает, что связи в молекуле смещаются между атомами, не оставляя при этом атомов и не добавляя к молекуле новых атомов. В сигматропической реакции замещающее вещество перемещается из одной части системы π в другую часть внутримолекулярной реакции с одновременной перегруппировкой системы π. Истинные сигматропические реакции обычно не нуждаются в катализаторе. Некоторые сигматропные реакции катализируются кислотой Льюиса. В сигматропных реакциях часто используются катализаторы переходных металлов, образующие промежуточные соединения в аналогичных реакциях. Наиболее известными сигматропными перегруппировками являются [3,3] Коповая перегруппировка, Клейзеновая перегруппировка, Кэрролловская перегруппировка и индоловый синтез Фишера.
Сигматропная перегруппировка
Обзор сигматропических сдвигов
Сдвиг сигматропической номенклатуры Вудвард-Хоффмана
Для описания сигматропических сдвигов используется специальная нотация. Каждому из атомов углерода на корешке молекулы присваивается порядковый номер. Сигматропические перегруппировки описываются порядковым номером [i,j]. Это означает миграцию атома σ, примыкающего к одной или нескольким системам π, в новое положение (i-1) и (j-1), удаленное от первоначального положения σ-связи. Когда сумма i и j является четным числом, это свидетельствует о вовлечении нейтральной, всей цепочки атомов C. Нечетное число говорит о том, что существует заряженный атом С или гетероатомная одиночная пара, заменяющая углерод-углеродную двойную связь. Таким образом, [1,5] и [3,3] сдвиги становятся [1,4] и [2,3] сдвигами с гетероатомами, сохраняя при этом соображения симметрии. В третьем примере гидрогены опущены для наглядности.

Вот способ найти порядок заданной сигматропической перестройки. Первый шаг - дать каждому атому числа, начиная с атомов разорванной связи как атома 1. Химики считают атомы в каждом направлении от разорванной связи к атомам, образующим новую σ-связь в продукте. Числа, соответствующие атомам, образующим новую связь, затем разделяются запятой и помещаются в скобки. Это создает дескриптор порядка сигматропических реакций.
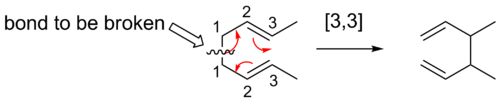
Химики также считают атомы, когда называют сигматропический сдвиг, в котором движется атом водорода. Цепь углерода не разрывается при миграции атома водорода. Таким образом, химики считают все атомы, участвующие в реакции, а не только ближайшие атомы. Например, следующая миграция атома водорода имеет порядок [1,5], достигаемый путем счета против часовой стрелки через систему π, а не порядок [1,3] через кольцевую группу CH2, который ошибочно получается, если считать по часовой стрелке.
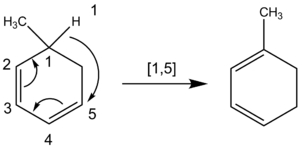
Супрафасциальные и антарафасциальные смены
Химики изучали сигматропные реакции, при которых мигрирующая группа имеет стероцентр. В принципе, все сигматропические сдвиги могут происходить при одинаковой (удерживание) или противоположной (инверсия) геометрии мигрирующей группы. Это зависит от того, используется ли исходная доля связи мигрирующего атома или другая его доля для формирования новой связи.
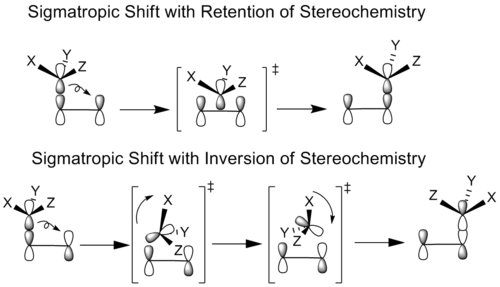
В случае стереохимического удерживания мигрирующая группа переводится без вращения в положение связи. В случае стереохимической инверсии мигрирующая группа как вращается, так и транслируется для достижения своей связной конформации.
Существует и другой способ, при котором в результате сигматропической реакции могут образовываться продукты с различной стерохимией. Мигрирующая группа может остаться на первоначальном лице системы π после переобучения. Или же она может перейти на противоположное лицо системы π. Если мигрирующая группа остается на том же лице системы π, то сдвиг называется надфациальным. Если мигрирующая группа переходит на противоположное лицо, то это называется антарафациальным сдвигом. Трансформации, происходящие внутри малых или средних колец, не могут приводить к антарафациальным сдвигам.
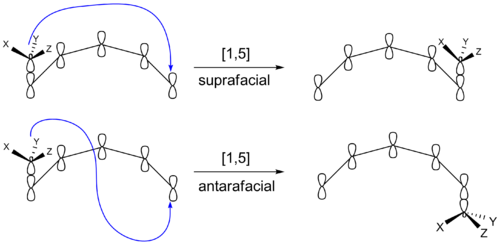
Классы сигматропических перегруппировок
[1,3] Сдвиги
Тепловые гидридные смещения
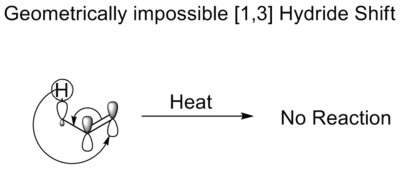
При тепловом [1,3] сдвиге гидрид перемещает три атома. Правила Вудвард-Хоффманна диктуют, что он будет двигаться в антарафациальном смещении. Хотя такой сдвиг допускается симметрией, топология Мёбиуса, требуемая в переходном состоянии, запрещает такой сдвиг. Это геометрически невозможно. Поэтому энолы не изомеризуются без кислотного или базового катализатора.
Тепловые алкиловые смещения
Тепловые алкильные [1,3] сдвиги, подобно [1,3] сдвигам гидридов, должны происходить антарафациально. Геометрия переходного состояния является запретительной. Но алкильная группа в силу природы своих орбиталей может инвертировать свою геометрию и сформировать новую связь с задней долей орбиты sp3. Эта реакция приведет к надфациальному сдвигу. Эти реакции до сих пор не распространены в открытых цепных системах из-за высокоупорядоченной природы переходного состояния. Таким образом, реакции лучше работают в циклических молекулах.
![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
Фотохимические [1,3] Сдвиги
Фотохимические [1,3] сдвиги должны быть надфациальными сдвигами, однако большинство из них несогласованны, так как проходят через триплетное состояние (т.е. имеют дирадикальный механизм, к которому правила Вудворд-Хоффмана не применимы).
[1,5] Сдвиги
Сдвиг [1,5] включает в себя сдвиг на 1 замену (-H, -R или -Ar) вниз на 5 атомов системы π. Было показано, что водород смещается как в циклических системах, так и в системах с открытой цепью при температурах не ниже 200 ˚C. Прогнозируется, что эти реакции будут протекать супрафациально, в переходном состоянии по гекелевой топологии.
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
Для фотооблучения потребовался бы антарафациальный сдвиг водорода. Хотя такие реакции встречаются редко, есть примеры, когда предпочтение отдается антарафациальным сдвигам:
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)
В отличие от водородных [1,5] сдвигов, в открытой системе никогда не наблюдалось [1,5] алкильных сдвигов. Химики определили скоростные предпочтения для [1,5] алкильных сдвигов в циклических системах: карбонильные и карбоксильные>гидридные>фениловые и винильные>>алкильные.
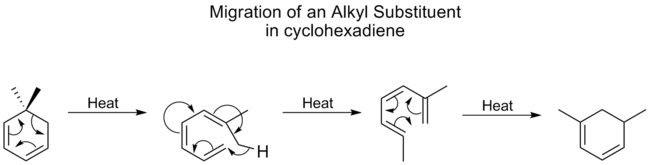
Алкильные группы претерпевают [1,5] смещения очень слабо и обычно требуют высоких температур. Однако для циклогексадиенов температура для алкильных сдвигов не намного выше, чем для карбонилов - лучшей мигрирующей группы. Исследования показали, что это происходит потому, что алкильные сдвиги на циклогексадиенах протекают по другому механизму. Сначала открывается кольцо, затем происходит сдвиг [1,7], а затем кольцо реформируется электроциклически:
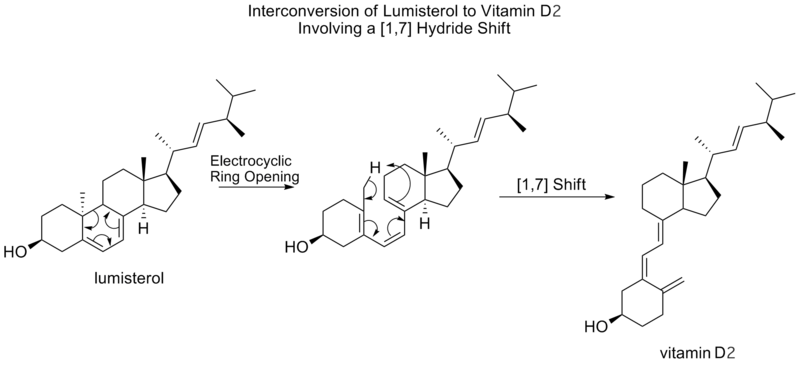
Этот же самый механистический процесс виден ниже, без окончательной электроциклической реакции закрытия кольца, в интерконверсии люмистерина в витамин D2.
[1,7] Сдвиги
[1,7] сигматропические сдвиги предсказываются правилами Вудфорда-Хоффмана, которые должны происходить антарафациально, переходным состоянием топологии Мёбиуса. Антарафациальный [1,7] сдвиг наблюдается при переходе люмистерина в витамин D2, где после раскрытия электроциклического кольца в превитамин D2 сдвигается метилводород.
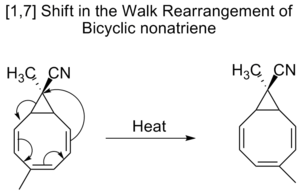
Велосипедные нонатриены также претерпевают [1,7] сдвиги в так называемой походной перестройке, которая представляет собой сдвиг двухвалентной группы, в составе трехчленного кольца, в велосипедной молекуле.
[3,3] Сдвиги
[3,3] сигматропические сдвиги являются хорошо изученными сигматропическими перегруппировками. Правила Вудфорд-Хоффмана предсказывают, что эти шесть электронных реакций будут протекать сверх-фациально, используя переходное состояние топологии Геккеля.
Клайсенское перераспределение
Открытая в 1912 году Райнером Людвигом Клейзеном, перестройка Клейзена является первым зафиксированным примером [3,3] -сигматропической перестройки. Эта перестройка представляет собой полезную реакцию образования связей углерод-углерод. Примером перегруппировки Клейзена является [3,3] перестройка аллил-винилового эфира, которая при нагревании дает γ,δ-ненасыщенный карбонил. Образование карбонильной группы делает эту реакцию, в отличие от других сигматропных перегруппировок, по сути необратимой.

Ароматическая перестройка Клейзена
Орто-клайсеновая перестройка включает в себя [3,3] смещение аллилфенилового эфира в промежуточное звено, которое быстро таутомеризуется в орто-замещенный фенол.
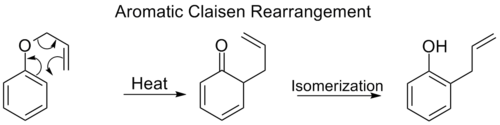
Когда оба ортопедических положения бензольного кольца заблокированы, происходит вторая ортопедическая перестановка. Эта пара-клайсеновая перестройка заканчивается таутомеризацией до три-замещенного фенола.
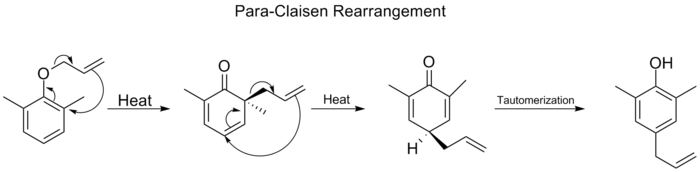
Перестройка копы
Перестройка копа представляет собой широко изученную органическую реакцию, включающую в себя [3,3] сигматропическую перестройку 1,5-диенов. Она была разработана Артуром К. Копом. Например, 3,4-диметил-1,5-гексадиен, нагретый до 300 °С, дает 2,6-октадиен.

перестройка Окси-копа
При перегруппировке Окси-копа гидроксильная группа добавляется при С3, образуя энал или энон после таутомерии кето-энола промежуточного энола:
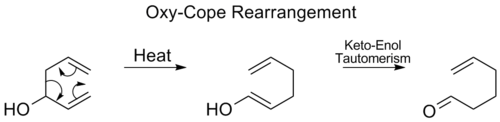
Перестановка каруселей
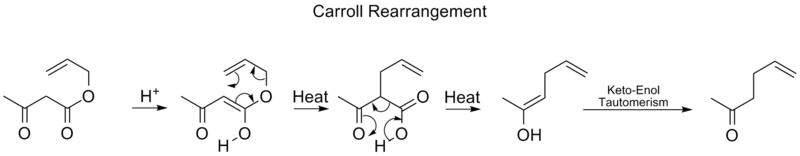
Реорганизация Кэрролла является реакцией перестройки в органической химии и включает в себя преобразование β-кето-аллилового аллильного эфира в α-аллил-β-кетокарбоновую кислоту. Эта органическая реакция может сопровождаться декарбоксилированием, и конечным продуктом является γ,δ-аллилкетон. Перестройка Кэрролла является адаптацией перестройки Клейзена и фактически декарбоксилирующим аллилированием.
синтез Фишера Индолы
Синтез индолов Фишера представляет собой химическую реакцию, в результате которой из (замещенного) фенилгидразина и альдегида или кетона в кислых условиях образуется ароматический гетероцикл индолов. Реакция была открыта в 1883 году Германом Эмилем Фишером.
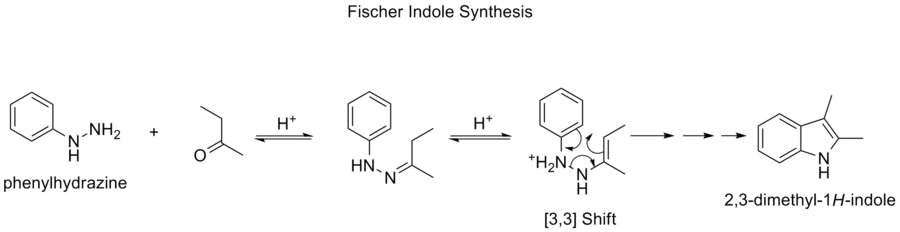
Выбор кислотного катализатора очень важен. Успешные кислотные катализаторы включают в себя: Бронстированные кислоты, такие как HCl, H2SO4, полифосфорная кислота и р-толуолуолусульфоновая кислота. Кислоты Льюиса, такие как трифторид бора, хлорид цинка, хлорид железа и хлорид алюминия также являются полезными катализаторами.
Было опубликовано несколько обзоров.
[5,5] Сдвиги
Подобно сдвигам [3,3], правила Вудфорд-Хоффмана предсказывают, что [5,5] сигматропические сдвиги будут протекать супрафациально, переходное состояние топологии Гекеля. Эти реакции встречаются реже, чем сигматропические сдвиги [3,3], но это в основном связано с тем, что молекулы, которые могут претерпевать [5,5] сдвиги, встречаются реже, чем молекулы, которые могут претерпевать [3,3] сдвиги.
![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)
Прогулки перегруппировки
Миграцию двухвалентной группы, такой как O, S, NR или CR2, которая является частью трехчленного кольца в молекуле велосипеда, обычно называют пешеходной перегруппировкой. В соответствии с правилами Вудвард-Хофмана это может быть формально охарактеризовано как (1, n) сигматропический сдвиг. Примером такой перестройки является сдвиг заместителей на тропилиденах (1,3,5-циклогептатриенах). При нагревании пи-система проходит через закрытие электроциклического кольца и образует велосипед[4,1,0]гептадиен (норкарадиен). Затем следует [1,5] алкильное смещение и открытие электроциклического кольца.
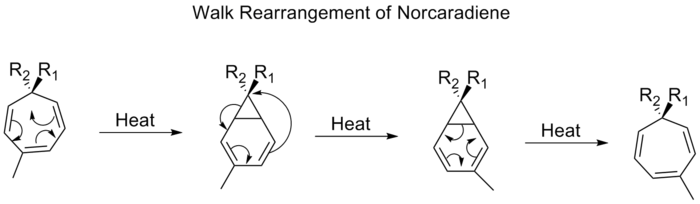
Проходя через [1,5] сдвиг, ожидается, что ходовая перегруппировка норкарадиенов будет проходить надфациально с сохранением стереохимии. Экспериментальные наблюдения, однако, показывают, что 1,5-сдвиги норкарадиенов идут антарафациально. Теоретические расчеты показали, что [1,5] смещение является дирадикальным процессом, но без привлечения дирадикальных минимумов на поверхности потенциальной энергии.
Связанные страницы
- 2,3-сигматропическая перестройка
- смена NIH
- Пограничная молекулярно-орбитальная теория
- правила Вудворд-Хоффманна
Вопросы и ответы
В: Что такое сигматропная реакция в органической химии?
О: Сигматропная реакция - это перициклическая реакция, которая включает некатализируемый внутримолекулярный процесс и изменяет одну σ-связь на другую σ-связь.
В: Включает ли сигматропная реакция катализатор?
О: Настоящая сигматропная реакция обычно не включает катализатор, хотя некоторые сигматропные реакции могут быть катализированы кислотой Льюиса.
В: Что означает термин "сигматропный"?
О: Термин "сигматропный" - это сложное слово, состоящее из слова "сигма", которое относится к одинарным углерод-углеродным связям, и греческого слова "тропос", означающего поворот.
В: Какой тип реакции является сигматропной?
О: Сигматропная реакция - это реакция перегруппировки, означающая, что связи в молекуле смещаются между атомами, при этом атомы не уходят и не добавляются новые атомы к молекуле.
В: Что происходит при внутримолекулярной сигматропной реакции?
О: При внутримолекулярной сигматропной реакции заместитель перемещается из одной части системы с π-связями в другую часть с одновременной перестройкой π-системы.
В: Существуют ли какие-либо хорошо известные сигматропные перегруппировки?
О: К наиболее известным сигматропным перегруппировкам относятся [3,3] перегруппировка Коупа, перегруппировка Клайзена, перегруппировка Кэрролла и синтез индола по Фишеру.
В: Часто ли в сигматропных реакциях используются катализаторы из переходных металлов?
О: Да, в сигматропных реакциях часто участвуют катализаторы из переходных металлов, которые образуют промежуточные продукты в аналогичных реакциях.